Новости
20 марта 2020 Новости
Data Management 365 экстренно представляет MainEDC™ COVID-19 Pack - валидированное решение, способное поддержать процесс клинических исследований в условиях пандемии.
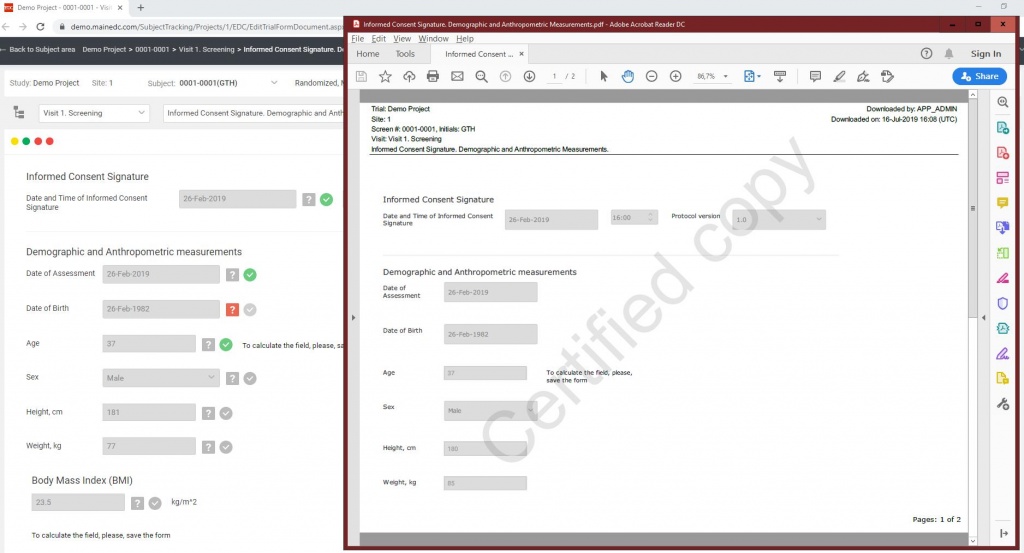
Удаленное мониторирование, включая возможность фотографии (или сканирования) первичной документации прямо из системы
Экстренные изменения в связи с возможными отклонениями от первоначального протокола
Изоляция медицинских учреждений
Перевод сотрудников на работу из дома
Поддержка преемственности процессов
Ускоренный старт проектов по COVID-19
Для всех наших текущих клиентов расширение MainEDC™ COVID-19 Pack предоставляется бесплатно !
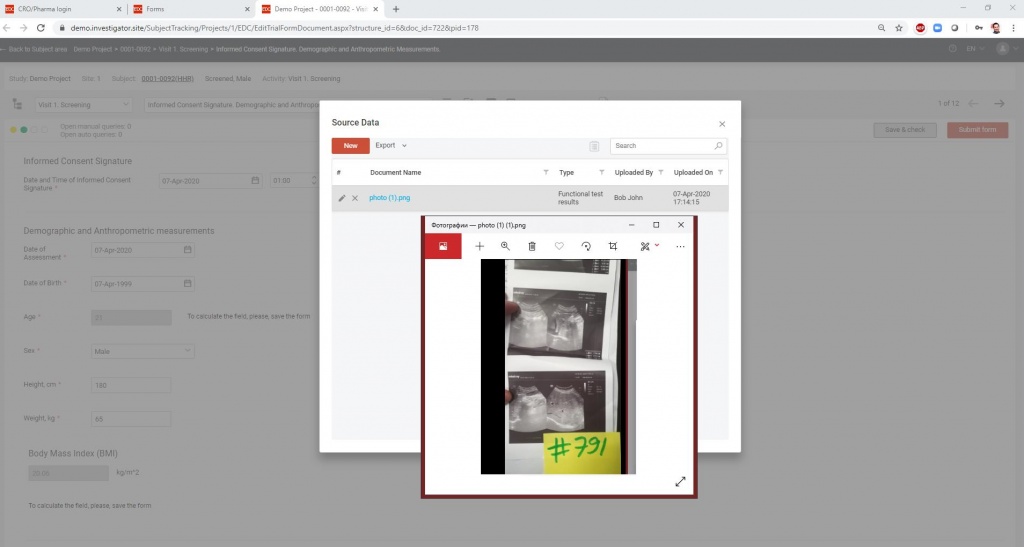
Наше предложение:
Инструменты реализации предложений FDA* по проведению клинических исследований в условиях пандемии**
Возможность полностью удаленной работы
24x7 с любого устройства
Мгновенный доступ проектной команды к введенным исследователями данным
Защищенный режим удаленного мониторирования - Source Documentation Review
Контроль проекта через регулярные E-mail отчеты
Поддержка процедуры полного отсутствия бумажных носителей в проекте
Валидированные электронные подписи
QA-сопровождение процессов исследования
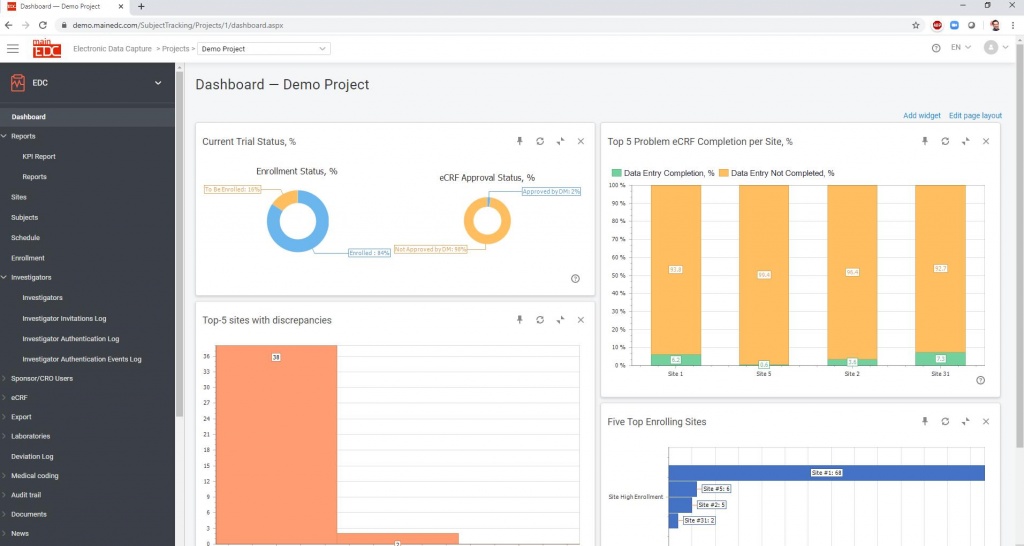
Вовремя информируйте ваших сотрудников и исследователей - Documents and Study News share Tool
Спонсор всегда держит руку на пульсе (ALCOAC)
Инструменты : Dashboard + KPI Report + Advanced Report Tool & 40 Predefined Reports
Экспорт данных в реальном времени в SDTM/SAS/XML/XLSX/CSV
WHODrug, MedDRA, ATC, ICD: кодирование и авто-кодирование в системе, диалог исследователь-кодировщик-медицинский монитор
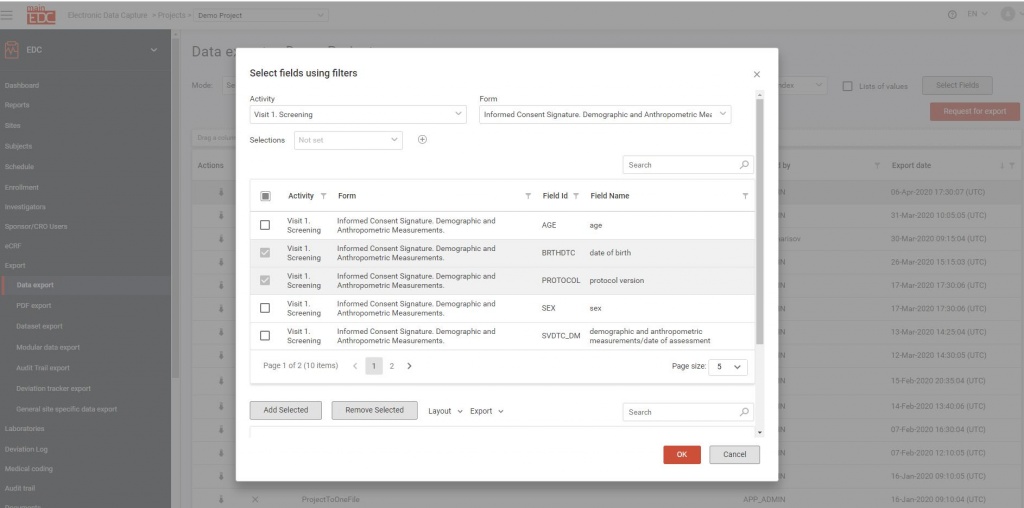
Быстрый старт вашего исследования по COVID-19
Значительно ускоренный запуск нового проекта
Полное клонирование проектов и отдельных частей
Онлайн согласование дизайна эИРК сразу в системе, без промежуточных макетов
Мгновенная реализация работ с изменениями к протоколу и версиями
Быстро изменяйте исследование под новые требования
Поддержка динамического дизайна
Полный контроль и изменения расписания визитов
Быстрый переход на EDC в проектах запущенных на бумажном ИРК
Изменение структуры проекта в любой момент исследования
Поддержка версионности протокола и информированного согласия
Поддержка рукавов и путей исследования
Поддержка гибридной модели исследования
Контролируйте отклонения
Лог отклонений от протокола в соответствии с новыми рекомендациями FDA*
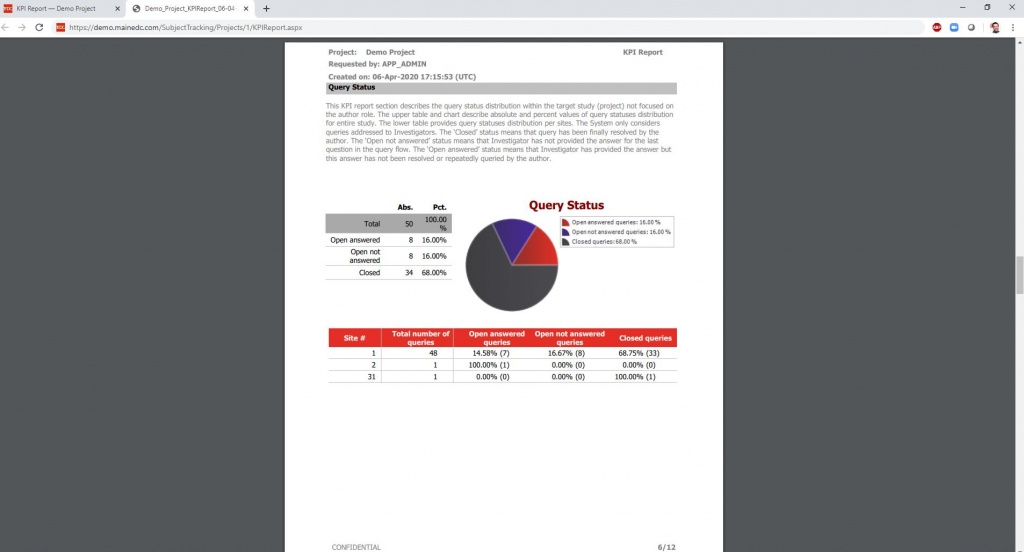
Изменяйте подходы к мониторированию
Динамические настройки RBM
SDV на любом уровне:
Поле, страница, визит, пациент, центр, страна
Гибкие правила для верификации, основанные на Site KPI Confidence, Interval Country/Area Rules, Investigator Assessment,
Одобрение только критических данных
Интеграция с 17 лабораториями и 24 производителями ПО, полная интеграция с Flex Databases CTMS
Мы поможем вам изменить конфигурацию системы для соответствия новым жизненным реалиям - предлагаем тренинг или консультацию
Наш опыт:
Более 1000 клинических исследований, проведенных на платформе
32 исследования с центральным мониторингом
114 исследования с Risk Based подходом
109 исследования с частичным SDV
218 исследований без мониторных визитов
100% наших клиентов используют RBM-driven KPI Report
4 проекта по COVID-19 уже в стадии настройки ИРК, рандомизации и логистики
47 проектов наших клиентов уже переведены на удаленное мониторирование из-за пандемии (* к 1 Мая 2020)
Предлагаем валидированное решение:
GCP E6 R2, GAМP 5, 21 CFR Part 11, GDPR, HIPAA
ГОСТ Р 52379-2005 «Надлежащая клиническая практика»
ГОСТ Р ИСО 14155-2014 «Надлежащая клиническая практика. Clinical investigations. Good clinical practice»
ФЗ-152, Лицензия Роскомнадзор (№ 78-19-005811)
Аккредитация Министерства связи и массовых коммуникаций РФ (№5538)
Система валидирована (36 Аудитов качества, IT и разработки)
9 валидированных и проверенных дата-центра по всему миру с управляемым оборудованием
Избыточная система кластеризации, репликации и резервного копирования
Полный электронный след на базе технологии блокчейн
Приложение запатентовано ( 5 патентов)
Дополнения к системе будут доступны вместе с еженедельным релизом 25 Марта 2020 г. Для включения необходимого функционала, пожалуйста, свяжитесь со службой поддержки для получения консультаций и UAT Scripts.
Хотите перестроить проект? support@mainedc.com
Хотите начать новый проект? contact@datatamanagement365.com
* FDA Guidance on Conduct of Clinical Trials of Medical Products during COVID-19 Pandemic
** Для получения дополнительных материалов, пожалуйста обратитесь к нам.
Ваша команда Data Management 365

Другие новости